がんによって全身に不調が生じるのはなぜか?
がんをもつ個体の肝臓の異常に焦点をあてる
【発表のポイント】
⚫ がんをもつマウス個体とがんをもたない個体の肝臓における遺伝子の発現量や代謝物の量を比較することで、がんによって生じる肝臓の異常の全体像を捉えました
⚫ 肝臓の代謝異常の一部において宿主のニコチンアミドメチル基転移酵素 (NNMT) (注1) が重要な役割を果たしていることを明らかにしました
⚫ がんによって全身に不調が生じるのはなぜなのかという問題に関する理解が深まり、不調を抑えこむ方法論の開発へとつながることが期待されます
【概要】
がんは身体にさまざまな異常 (体重減少や代謝異常など) をひきおこします。その根幹は、がんが離れた位置にある宿主臓器や細胞に作用できる、ということにあります。この作用は極めて複雑で、その実態やメカニズムに関する私たちの理解は限定的です。東北大学 加齢医学研究所 生体情報解析分野 河岡慎平准教授 (京都大学 医生物学研究所 臓器連関研究チーム 特定准教授を兼務) の研究グループは、東京大学、九州大学、京都大学の研究チームとの共同研究により、がんが、離れた位置にある肝臓でニコチンアミドメチル基転移酵素 (NNMT) の発現量を増加させ、このことによって多様な代謝異常をひきおこしていることを見出しました。NNMTを欠失させたマウスではがんによる肝臓の異常の一部が緩和され、全身性の不調も部分的に抑制されていました。本研究により、がんが身体に不調をもたらすしくみの一端が明らかとなりました。本成果ががんに起因する不調の全体像を理解する一助となり、また、不調を強力に抑えこむ方法論の開発につながることが期待されます。
本研究成果は2022年6月15日に英国の学術誌であるNature Communicationsに掲載されます。
図2 がん→NNMT→ウレア回路の抑制というしくみの発見
【問い合わせ先】
東北大学加齢医学研究所 生体情報解析分野
担当:河岡 慎平
電話番号:022-717-8568
E-mail:shinpei.kawaoka.c1*tohoku.ac.jp
(*を@に置き換えてください)


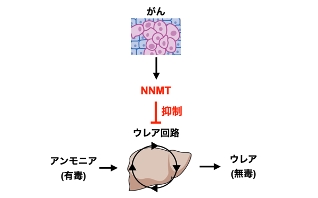



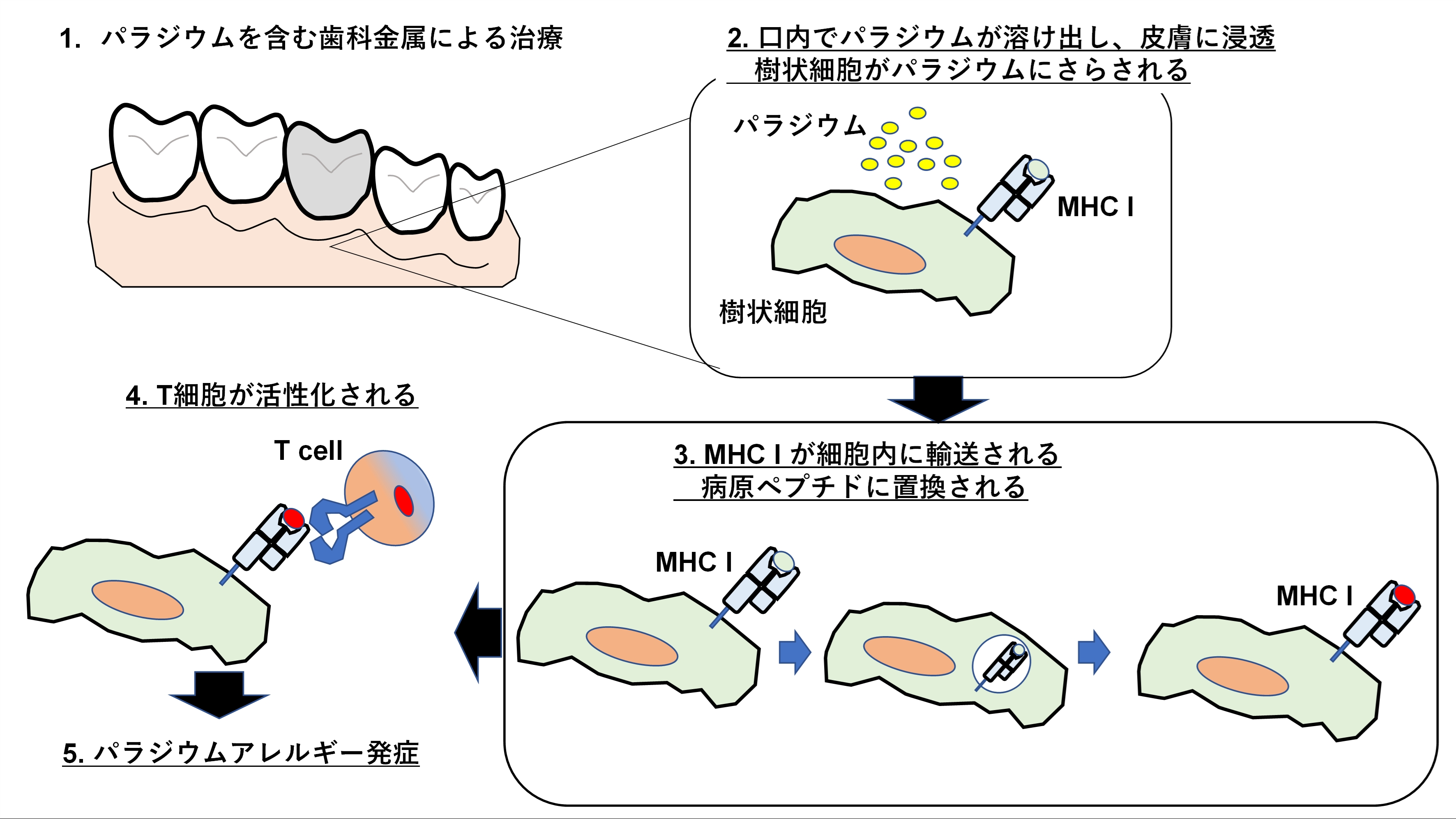 図. パラジウムによる金属アレルギー誘導機構
図. パラジウムによる金属アレルギー誘導機構