| 教授 | 博士 小笠原 康悦 |
| 助教 | 博士 渡辺 数基 |

当研究分野は、平成20年7月に加齢生体防御学研究分野として新設されました。その後、加齢医学研究所の部門再編に伴い、平成22年4月より、生体防御学分野として名称変更いたしました。加齢医学研究所では、加齢医学を「受精から発生・発達・成熟・老化に至る時間軸に沿った医学・生物学」と定義し、加齢のメカニズムや加齢を制御する生体防御機構を解明すること(基礎加齢研究)、および加齢に伴う疾患(認知症などの脳・神経疾患や難治性がん)に関する先端的診断・治療法の開発を行い、社会が要請するこれら重要疾患の克服を目指しています。この研究所のミッションの一翼を担うべく、当分野では、生体防御機構について研究をしています。
当研究室では、加齢に伴う免疫異常が原因となっている、がん、自己免疫疾患、感染症などについてNK細胞およびT細胞の認識機構に焦点を当てて、免疫システムを研究しています。我々は、動物モデル、遺伝子組み換え技術を用いてこれら疾患の病態を明らかにし、新規診断・治療法の開発を目指しています。
我々が着目しているNK細胞は、自然免疫系および獲得免疫系の両方で活躍しており、ウイルス感染細胞の排除やがん細胞の排除に深くかかわっています。NK細胞は、これら標的細胞を活性化レセプターと抑制性レセプターの2つのレセプターで認識していることが知られています。我々はこのレセプターの認識機構に焦点を当てて研究をしています。最近、NK活性化レセプターNKG2Dが、ウイルス感染症、腫瘍免疫、自己免疫性糖尿病に関与していることを明らかにしました。
我々は、これらの研究に興味がある学生を広く受け入れ、研究の面白さ、醍醐味をぜひ味わっていただきたいと思っております。
現在の主な研究
1)腫瘍免疫の研究
がんは、放射線や化学物質によるDNA損傷や、ウイルス感染、遺伝子発現制御の異常など種々の要因により引き起こされることが知られています。免疫系はこれら発がん細胞を排除すべく監視にあたっています。がん細胞は、常に免疫系から排除される選択圧を受けていて、がん細胞の遺伝的不安定性とあいまって、悪性度を高めていくというImmuno-editingとよばれる概念が提唱されています。我々は、Immuno-editingを証明するために、動物モデル、遺伝子組み換え技術を用いて、特に、NK細胞レセプターNKG2Dに着目して研究を進めています。
活性化レセプターであるNKG2DはNK細胞の主たるレセプターとして、腫瘍免疫や病原微生物に対する免疫応答にかかわっています。興味深いことに、悪性腫瘍でNKG2Dリガンドが広く発現していることが知られており、なぜ悪性腫瘍が免疫監視をすりぬけることができるのか不明でした。我々は、NK細胞上のNKG2Dとリガンドとの相互作用がNK細胞の機能不全を引き起こすことを発見しました。NK細胞とNKG2Dリガンドを発現している腫瘍細胞との最初の反応では、NK細胞は腫瘍細胞を傷害し、サイトカインも産生できます。しかし、しばらくリガンドにさらされると、腫瘍細胞はNKG2Dのdown modulationを誘導します。すなわち、リガンドとの暴露でNK細胞を機能不全に導くと考えられます。このことは、腫瘍の進展の過程で、NK細胞が機能不全におちいる現象を説明できる結果であり、また、悪性腫瘍が免疫監視をすりぬけることができる現象を説明できる結果です(Figure 1, Immunity 2003)。
2)自己免疫疾患の研究
I型糖尿病は、自己反応性T細胞により膵臓のインスリン産生細胞が破壊されることにより発症する疾患です。NODマウスは、I型糖尿病のモデル動物として有用であり広く用いられています。最近、我々はNKG2Dリガンドの1つ、RAE-1が前糖尿病段階のNODマウス膵臓で発現していること、および膵臓に浸潤している自己反応性CD8+T細胞がNKG2Dを発現していることを発見しました。抗NKG2D抗体の投与により、前糖尿病段階のNODマウスにおいても糖尿病の発症を完全に抑制できることを報告しました(Figure 2, Immunity 2004)。この発見は、NKG2DがI型糖尿病の新たな治療標的になりうることを示したものです(Nature Medicine, Nature Reviews, Reutersほか10報道)。この発見をもとにして、現在、アメリカで臨床治験が始まっています。
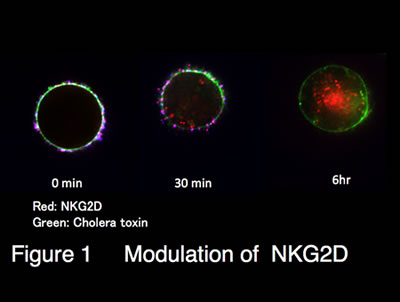
図1

図2
3)金属アレルギーの研究
ネックレスなど装飾品をつける人の増加により、金属アレルギー患者は増加の一途にあります。金属は食物にも含まれており、生活をする上で金属に触れないようにすることは極めて困難であることから、社会問題化しています。金属アレルギーは、T細胞依存性のIV型アレルギーと位置付けられておりますが、その実態は不明のままです。我々は、厚生労働省研究班を組織し、皮膚科学、歯学、薬学、工学、素材工学の研究者とともに金属アレルギーの病態解明、新規診断法の開発、新規医用材料の開発を目指して研究をすすめています。本研究班は、金属アレルギーの発症の分子機構を解明するため金属アレルギー動物モデルを確立することに成功しました。この成果はNature誌に記事として取り上げられ世界的にも高く評価されています。

